Hidratos de carbono (Pignataro)- ADN (Canepa) - Krebs (Calvo)
Hidratos de carbono (Prof. Pignataro)
1) Escriba las estructuras químicas (Fischer o Haworth) de la lactosa y de la fructosa 6 fosfato.
2) En una comida un individuo ingiere 180g de almidón que está formado por 50% de cada uno de sus dos polisacáridos componentes. Ambos polisacáridos tienen una masa molar de 9.10^6 g/mol. Suponga que todo el almidón ingerido es utilizado exclusivamente como fuente de energía por el músculo en anaerobiosis, que los dos polisacáridos se catabolizan totalmente (100%) y que todas las enzimas actúan correctamente para degradar el almidón.
En el polisacárido 2, el 20% de los monómeros forman parte de ramificaciones. Los monómeros constituyentes, independientemente de que uniones puedan tener, tienen una masa molar promedio de 180 g/mol.
Considere que ambos polisacáridos son degradados de la misma manera y por las mismas enzimas que actúan sobre el glucógeno y que dicha degradación es regulada exactamente igual por metabolitos y hormonas.
Calcule:
a) cuantos moles de producto/s final/es se obtendrán.
b) cuantos moles de ATP se obtendrán.
3) Dé solamente el nombre de todas las enzimas reguladas por metabolitos u hormonas de la glucólisis, gluconeogénesis, vía de las pentosas y metabolismo del glucógeno en todos los tejidos.
4) De las enzimas que mencionó en el punto anterior, elija dos de diferentes vías metabólicas y que no catalicen pasos opuestos y explique en el espacio marcado abajo mediante un esquema o muy brevemente como es el mecanismo de regulación para la hormona glucagón.
ADN (Prof. Canepa)
1) (3 puntos)
Responder justificadamente:
a) ¿Cuál es el significado de la Tm del ADN? ¿Cómo y por qué varía la Tm con la composición de bases distintas de ADN?
b) ¿Cómo y por qué varía la Tm de un ADN con la fuerza iónica de la solución en la que se encuentra?
c) ¿Cuál es el fundamento químico en el que se basa la distinta estabilidad del ARN y ADN?
2) (4 puntos)
El DNA se encuentra dentro del núcleo organisado como estructura cromatínica formando nucleosomas.
a) Describir la composición del nucleosoma y de qué modo está organizado en el núcleo celular.
b) ¿Cuál es el significado en términos de la regulación génica de esta estructura cromatínica? ¿Por qué?
c) ¿Cuál es la razón por las que las proteínas histonas interaccionan fuertemente con el ADN? ¿Por qué la acetilación de histonas modifica esta interacción?
d) ¿A través de qué mecanismos puede modificarse la interacción del ADN con las histonas?
3) (4 puntos)
Se sabe que el factor de transcripción E2F1 se une al promotor del gen PRX en células neuronales del hipocampo de ratones normales. Se analiza la unión de E2F1 a este promotor en ratones que han sido sometidos a un intenso estrés. Paralelamente, se realiza el mismo estudio en ratones sometidos al mismo estrés pero tratados con DEC, un fármaco que inhibe todas las ADN metiltransferasas.
Para estudiar la unión de E2F1 al promotor de PRX se ha utilizado la técnica de ChIP (inmunoprecipitación de la cromatina). Tambiénse analiza la unión de E2F1 al promotor del gen DRO, un gen del cual ya se sabe que une E2F1, y al promotor del gen URA, ya conocido por no unir E2F1. Por otro lado se determina la cantidad de mRNA de PRX en hipocampo de ratones normales o tratados. Los resultados se muestran en las figuras:
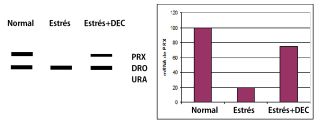
a) Que indican los resultados del ChIP en relación con la unión del E2F1 al promotor de PRX.
b) Por qué se incluye el estudio de la unión de E2F1 a DRO y URA si ya es conocido.
c) Analizar los resultados de ChIP con los de presencia de mensajero y metilación del ADN y exponer una hipótesis que los integre.
Krebs (Prof. Calvo) -> con respuestas, gracias a su amabilidad!
Pregunta 1: sabiendo que la degradación mitocondrial de ácidos grasos de cadena par rinde unidades de acetil-CoA y de cadena impar rinde acetil-CoA y propionil-CoA que se metaboliza a succinil-CoA, ¿cuál/es será/n reacciones anapleróticas y por qué? (2 puntos).
Respuesta: Dado que la degradación mitocondrial de ácidos grasos de cadena impar rinde, además de acetilCoA, también propionilCoA que se metaboliza a succinilCoA, este metabolismo sí resultará anaplerótico porque la succinilCoA es uno de los intermediarios del ciclo de Krebs. La acetilCoA por sí sola no resulta anaplerótica.
Pregunta 2: cuando Stefan succione la sangre de Elena y el acetilo marcado ingrese en Krebs, ¿saldrán marcadas en la primera vuelta las moléculas de CO2? Justifique (1 punto).
Respuesta: los carbonos que ingresan del acetilo, no salen en la primera vuelta de Krebs, sino que son los del oxalacetato. En la segunda vuelta salen los carbonos correspondientes al carbonilo y a partir de la tercera vuelta los del metilo del acetilo. Los carbonos del CO2 que salen en la primera vuelta son del oxalacetato.
Pregunta 3: sabiendo que el ATP disminuye la afinidad de la piruvato deshidrogenasa (E1) por el TPP (pirofosfato de tiamina), ¿consideraría esto una cooperatividad homotrópica/heterotrópica positiva/negativa? Justifique (1 punto).
Respuesta: si el ATP disminuye la afinidad de la enzima por el TPP se puede considerar una cooperatividad heterotrópica (entre moléculas diferentes) negativa (disminuye la afinidad). Dado que el TPP funciona como grupo prostético, la disminución en afinidad puede resultar en menor incorporación de la coenzima o en un cambio conformacional que diminuya la eficiencia de su uso.
Pregunta 4: el cianuro inhibe la cadena respiratoria, ¿cómo explica que esta inhibición resulte en que también se inhiba el Ciclo de Krebs? (2 puntos).
Respuesta: al inhibir el cianuro la cadena respiratoria, en el complejo II (succinato deshidrogenasa del ciclo de Krebs) no se puede regenerar el FAD, quedando como FADH2 y por lo tanto se frena el ciclo de Krebs.
Pregunta 5: utilizando el modelo de Monod o concertado, explique cómo el 2,3-BPG induce la cooperatividad homotrópica positiva para el oxígeno en su unión a la hemoglobina (1 punto).
Respuesta: en ausencia del BPG la hemoglobina presenta una cinética de asociación para el O2 hiperbólica. En presencia de BPG, según el modelo de Monod, esta molécula se unirá a la forma T (tensa o inactiva) y desplazará el equilibrio hacia ese lado. Ahora, el O2 al unirse a la forma R (relajada o activa) volverá a desplazar el equilibrio hacia esta forma resultando en la cooperatividad homotrópica positiva que es clásica en la función de la hemoglobina. En ausencia de BPG prácticamente toda la enzima estaba en la forma R y por eso el O2 no mostraba esa cooperatividad.
Pregunta 6: La sangre que está analizando tiene hemoglobina radiactiva. Sabiendo que el succinil-CoA es un metabolito para la síntesis del grupo hemo, ¿a quién pertenece la sangre? (0.5 puntos), ¿cómo apareció en la hemoglobina? (0.5 puntos). Justifique.
Respuesta: La sangre, como muy bien dijeron dos alumnos, puede pertenecer tanto a Elena como a Stefan. Todo depende de si la sangre goteó de los colmillos de Stefan o si fue producto de una lastimadura del vampiro (como esto era un divertimento, todos van a recibir los 0.5 puntos). Ahora bien, como en principio era el acetato de la acetilCoA el que estaba marcado, en ciclo de Krebs aparecerá marcada la succinilCoA y como este ciclo aprovisiona de intermediarios a otros metabolismos, entre ellos el de las porfirinas, por lo tanto la hemoglobina en su grupo hemo aparecerá marcada radiactivamente.
Pregunta 7: el NADH inhibe la reacción del complejo piruvato deshidrogenasa, ¿qué tipo de inhibición ejerce y sobre qué enzima del complejo? ¿Pasaría lo mismo con el complejo de la α-cetoglutarato deshidrogenasa? ¿Cómo lo explica? (1 punto). Dibuje la fórmula química del oxalacetato (0.5 puntos) e indique la característica del mecanismo de la reacción entre esta molécula y acetil-CoA, indicando el nombre de la enzima (0.5 puntos).
Respuesta: el NADH es el producto de la reacción de E3 en el complejo piruvato deshidrogenasa y encargada de devolver al ácido lipoico a su forma activa (puente disulfuro) como también de regenerar el FAD. Por lo tanto, la inhibición que ejerce el NADH es por producto sobre E3 (dihidrolipoil deshidrogenasa). Dado que el complejo de la α-cetoglurarato deshidrogenasa también posee la enzima E3, el NADH ejercerá el mismo efecto. La fórmula química del oxalacetato es
Y la enzima que cataliza la condensación de esta molécula con el acetilo de la AcetilCoa es la citrato sintasa que se caracteriza por presentar un mecanismo cinético secuencial ordenado. Primero debe unirse el oxalacetato a su sitio activo para que se forme el sitio para acetilCoA. Si no está presente el oxalacetato no se puede unir el acetilCoA. Es un mecanismo similar al que vimos para inhibidores incompetitivos.
